Effect of Preoperative Calcitriol Administration on Postoperative Hypocalcemia in Dialysis Patients Undergoing Parathyroidectomy: A Randomized Controlled Trial
Main Article Content
Abstract
Background: Secondary hyperparathyroidism is a common complication in patients with end-stage renal disease receiving dialysis, and parathyroidectomy is often required when medical treatment fails. Postoperative hypocalcemia is a frequent and serious complication that contributes to morbidity and prolonged hospitalization. This study aimed to determine whether preoperative administration of calcitriol reduces the severity of postoperative hypocalcemia and the need for parenteral calcium supplementation in dialysis patients undergoing parathyroidectomy.
Method: A single-center, open-label randomized controlled trial was conducted in 26 dialysis patients with severe secondary hyperparathyroidism. Participants were randomly assigned in a 1:1 ratio to receive either calcitriol 2 micrograms per day combined with calcium carbonate 3.6 grams per day for three days before surgery (intervention group, n=13) or calcium carbonate alone (control group, n=13). All patients were followed with serial calcium measurements for at least 72 hours after surgery. The primary outcome was the nadir serum calcium level within 24 hours postoperatively.
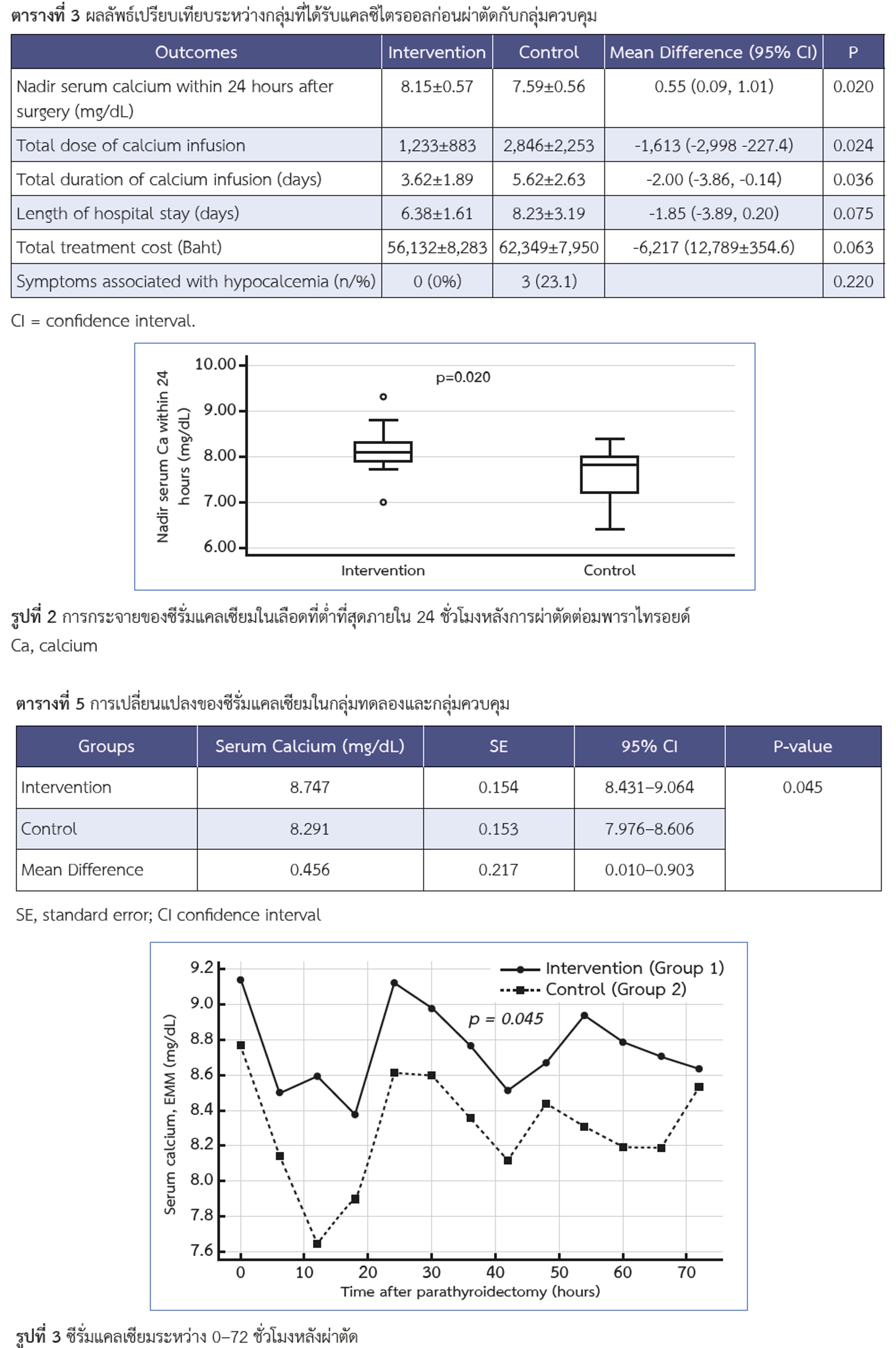
Result: Baseline characteristics were similar between groups. The intervention group showed significantly higher nadir serum calcium within 24 hours (8.15±0.57 vs. 7.59±0.56 mg/dL; p=0.020). The intervention group also required a lower total dose of intravenous calcium infusion (1,232.8±883.0 vs. 2,845.5±2,253.2 mg; p=0.024) and a shorter duration (3.6±1.9 vs. 5.6±2.6 days; p=0.036).
Conclusions: Short-term preoperative administration of calcitriol reduced the severity of postoperative hypocalcemia and decreased the requirement for intravenous calcium infusion in dialysis patients undergoing parathyroidectomy. These findings support the role of calcitriol as an effective perioperative strategy, although larger studies are needed to confirm long-term outcomes.
Article Details

This work is licensed under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
This article is published under CC BY-NC-ND 4.0 license, which allows for non-commercial reuse of the published paper as long as the published paper is fully attributed. Anyone can share (copy and redistribute) the material in any medium or format without having to ask permission from the author or the Nephrology Society of Thailand.
References
van der Plas WY, Noltes ME, van Ginhoven TM, Kruijff S. Secondary and Tertiary Hyperparathyroidism: A Narrative Review. Scand J Surg. 2020;109(4):271-8. doi: 10.1177/1457496919866015
Kim SM, Long J, Montez-Rath ME, Leonard MB, Norton JA, Chertow GM. Rates and Outcomes of Parathyroidectomy for Secondary Hyperparathyroidism in the United States. Clin J Am Soc Nephrol. 2016;11(7):1260-7. doi: 10.2215/cjn.10370915
Lau WL, Obi Y, Kalantar-Zadeh K. Parathyroidectomy in the Management of Secondary Hyperparathyroidism. Clin J Am Soc Nephrol. 2018;13(6):952-61. doi: 10.2215/cjn.10390917
Oliveira RBd, Silva ENd, Charpinel DMF, Gueiros JEB, Neves CL, Sampaio EdA, et al. Secondary hyperparathyroidism status in Brazil: Brazilian census of parathyroidectomy. Brazilian Journal of Nephrology. 2011;33(4):457-62. doi: 10.1590/s0101-28002011000400011
Jain N, Reilly RF. Hungry bone syndrome. Curr Opin Nephrol Hypertens. 2017;26(4):250-5. doi: 10.1097/mnh.0000000000000327
Gao D, Lou Y, Cui Y, Liu S, Cui W, Sun G. Risk factors for hypocalcemia in dialysis patients with refractory secondary hyperparathyroidism after parathyroidectomy: a meta-analysis. Ren Fail. 2022;44(1):503-12. doi: 10.1080/0886022x.2022.2048856
Cao L, Sun X, Zhang T, Niu Y, Suo H, Zhao Z, et al. A reappraisal of risk factors for early hypocalcemia after parathyroidectomy in dialysis patients. Updates Surg. 2022;74(6):1961-70. doi: 10.1007/s13304-022-01395-2
Silarat P, Saeseow S, Pathumarak A, Srisuwarn P, Suvikapakornkul R, Disthabanchong S. Improved Clinical Outcomes Associated With Hungry Bone Syndrome Following Parathyroidectomy in Dialysis Patients. Endocr Pract. 2024;30(11):1079-88. doi: 10.1016/j.eprac.2024.08.004
Sun X, Zhang X, Lu Y, Zhang L, Yang M. Risk factors for severe hypocalcemia after parathyroidectomy in dialysis patients with secondary hyperparathyroidism. Sci Rep. 2018;8(1):7743. doi: 10.1038/s41598-018-26142-9
Salman MA, Rabiee A, Salman AA, Youssef A, Shaaban HE, Ftohy T, et al. Role of vitamin D supplements in prevention of hungry bone syndrome after successful parathyroidectomy for primary hyperparathyroidism: A prospective study. Scand J Surg. 2021;110(3):329-34. doi: 10.1177/1457496920962601
Yuan Q, Liao Y, Zhou R, Liu J, Tang J, Wu G. Subtotal parathyroidectomy versus total parathyroidectomy with autotransplantation for secondary hyperparathyroidism: an updated systematic review and meta-analysis. Langenbecks Arch Surg. 2019;404(6):669-79. doi: 10.1007/s00423-019-01809-7
Shoback D. Clinical practice. Hypoparathyroidism. N Engl J Med. 2008;359(4):391-403. doi: 10.1056/NEJMcp0803050
Pérez A, Picotto G, Carpentieri A, Rivoira M, López M, Talamoni N. Minireview on regulation of intestinal calcium absorption. Emphasis on molecular mechanisms of transcellular pathway. Digestion. 2008;77:22-34. doi: 10.1159/000116623
Niramitmahapanya S, Sirirachta C, Niramitmahapanya BL, Deerochanawong C, Krairitichai U, Athipan P. Comparison effect of loading calcitriol and titrating calcitriol treatment to control hypocalcemia after parathyroidectomy in chronic kidney disease: randomized control trial, open labeled. J Med Assoc Thai. 2014;97 Suppl 11:S56-61.
Alsafran S, Sherman SK, Dahdaleh FS, Ruhle B, Mercier F, Kaplan EL, et al. Preoperative calcitriol reduces postoperative intravenous calcium requirements and length of stay in parathyroidectomy for renal-origin hyperparathyroidism. Surgery. 2019;165(1):151-7. doi: 10.1016/j.surg.2018.03.029
Ferreira D, Vilayur E, Gao M, Sankoorikal C, Bendinelli C. Calcitriol loading before total parathyroidectomy with autotransplant in patients with end-stage kidney disease: does it prevent postoperative hypocalcaemia? Intern Med J. 2019;49(7):886-93. doi: 10.1111/imj.14209
Grube M, Weber F, Kahl AL, Kribben A, Mülling N, Reinhardt W. Effect of High Dose Active Vitamin D Therapy on the Development of hypocalcemia After Subtotal Parathyroidectomy in Patients on Chronic Dialysis. Int J Nephrol Renovasc Dis. 2021;14:399-410. doi: 10.2147/ijnrd.S334227
Ho LY, Wong PN, Sin HK, Wong YY, Lo KC, Chan SF, et al. Risk factors and clinical course of hungry bone syndrome after total parathyroidectomy in dialysis patients with secondary hyperparathyroidism. BMC Nephrol. 2017;18(1):12. doi: 10.1186/s12882-016-0421-5.
Ketteler M, Block GA, Evenepoel P, Fukagawa M, Herzog CA, McCann L, et al. Executive summary of the 2017 KDIGO Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD) Guideline Update: what’s changed and why it matters. Kidney Int. 2017;92(1):26-36. doi: 10.1016/j.kint.2017.04.006
Jameson JL, Kasper DL, Longo DL, Fauci AS, Hauser SL, Loscalzo J. Harrison’s principles of internal medicine2018.
Serdar CC, Cihan M, Yücel D, Serdar MA. Sample size, power and effect size revisited: simplified and practical approaches in pre-clinical, clinical and laboratory studies. Biochem Med (Zagreb). 2021;31(1):010502. doi: 10.11613/bm.2021.010502
Steinl GK, Kuo JH. Surgical Management of Secondary Hyperparathyroidism. Kidney Int Rep. 2021;6(2):254-64. doi: 10.1016/j.ekir.2020.11.023
Gram J, Junker P, Nielsen HK, Bollerslev J. Dose-response effect of short-term calcitriol treatment on bone and mineral metabolism in normal males. Bone. 1996;18(6):539-44. doi: 10.1016/8756-3282(96)00074-9
Dream S, Kuo LE, Kuo JH, Sprague SM, Nwariaku FE, Wolf M, et al. The American Association of Endocrine Surgeons Guidelines for the Definitive Surgical Management of Secondary and Tertiary Renal Hyperparathyroidism. Ann Surg. 2022;276(3):e141-e76. doi: 10.1097/sla.0000000000005522
Lorenz K, Bartsch DK, Sancho JJ, Guigard S, Triponez F. Surgical management of secondary hyperparathyroidism in chronic kidney disease--a consensus report of the European Society of Endocrine Surgeons. Langenbecks Arch Surg. 2015;400(8):907-27. doi: 10.1007/s00423-015-1344-5
K/DOQI clinical practice guidelines for bone metabolism and disease in chronic kidney disease. Am J Kidney Dis. 2003;42(4 Suppl 3):S1-201.